2025年臨床研究專員
(Clinical Research Associate, CRA)
專業實務訓練課程
課程說明: 新藥臨床試驗當前已成世界性顯學!世界各國政策均強調臨床研究研發以因應險峻局
勢,我國卓越臨床試驗研發質量卓越,亦獲世界各國稱許;健保署籌設新台幣100億元新藥
基金,更為臨床試驗產業注入強心針,其中人員訓練即為其中重要環節。
臨床研究專員(CRA)薪資在各行業排名中名列前茅,五大產業創新研發計畫中亦包含積
極推動生物科技產業政策,現今國內外藥廠、CRO、醫材廠商、生技公司等相關產業對CRA
人才需求孔急,為相關學經歷背景者提供最佳職涯發揮平台。
本課程為台灣極寶貴之專業實務訓練課程,以Global Reach, Local Expertise為課
程設計目標,提供無經驗或初任或資深CRA之學員提供全方位藥品、醫材、食品臨床研究
及CRA角色功能指導。內容可提供生技產業新職涯選擇之整備,藉助豐富經驗的實務講師
提供逐步指導、獨到的工作手冊等寶貴資訊可供立即運用於CRA工作或謀職利器。
課程涵蓋CRA工作必備職能,遵循ICH GCP法規架構,師資成員延聘自醫療機構院長、
總監顧問、著名藥廠、CRO及醫學中心卓具實務經驗高階主管。提供有意加入CRA 工作卻不
知如何切入者或機構彌補專業訓練缺口、學界欲轉業界者及年資2年內亟盼業務精
進者均提供難得的學習機會!小班式教學,名額有限,請有志者把握難得的機會報名,全
程參與者生技中心(DCB)將提供學員精美上課證書並贈送CRA工作手冊,課程證明可供臨床
試驗執行及送審法規所需12小時GCP必要學分時數,獲致專業職能提升,加強面談自信。
二天課程期間現場同步另邀博士級資深顧問,免費提供就業及專業領域諮詢協助。
課程特色:
- 醫療機構及業界專家面對面實體互動授課
- 國際同步職場實例講解及實踐問題解決導向學習活動
- 提供實務工作運用為基礎內容,協助學員工作場域之工具
- 提供專業課程時數證明,符合國內法規需求
課程目標:
1. 強調CRA的核心能力,按部就班指導始文件驗證、試驗案時間管理及訪視準備
2. 掌握溝通、領導力與試驗機構互動:臨床研究專員的必備技能
3. 工具指導CRA各階段新藥開發與臨床試驗設計精隨,通盤瞭解計畫書內容重點
4. 進行臨床試驗合約剖析及計畫預算編列與協商經驗分享,縮短議約期程並減少試驗案損失
5. 徹底指導臨床試驗監測訪視報告撰寫,以及如何做好稽核與查核的準備,創造共贏
6. 親身分享如何智選試驗機構及可行性分析確保試驗案成功,提供學員從業參考
7. 首創主席親自指導臨床試驗資料及安全性監測委員會的角色與運作實務,精進執行知能
8. 分享實務臨床試驗的品質管制、品質保證正確措施,輔以國際最新風險為基礎監測技巧
建議學員:1. 任職生技業CRA之 In-house或Field-based CRA欲再精進者
2. 目前任職臨床研究相關產業(CRO、生技公司、藥廠、醫材廠商、精準醫療、醫院、研
究機構等),想要嘗試或瞭解不同角色職責者
3. 其他尚無經驗,未來有意進入藥品、醫材、食研、醫研臨床試驗工作領域之醫藥相關
人士及應屆畢業學生,需要謀職之專業知識技能者
4.缺乏臨床試驗GCP時數者或生醫及臨床試驗領域相關機構提供員工在職訓練需求者
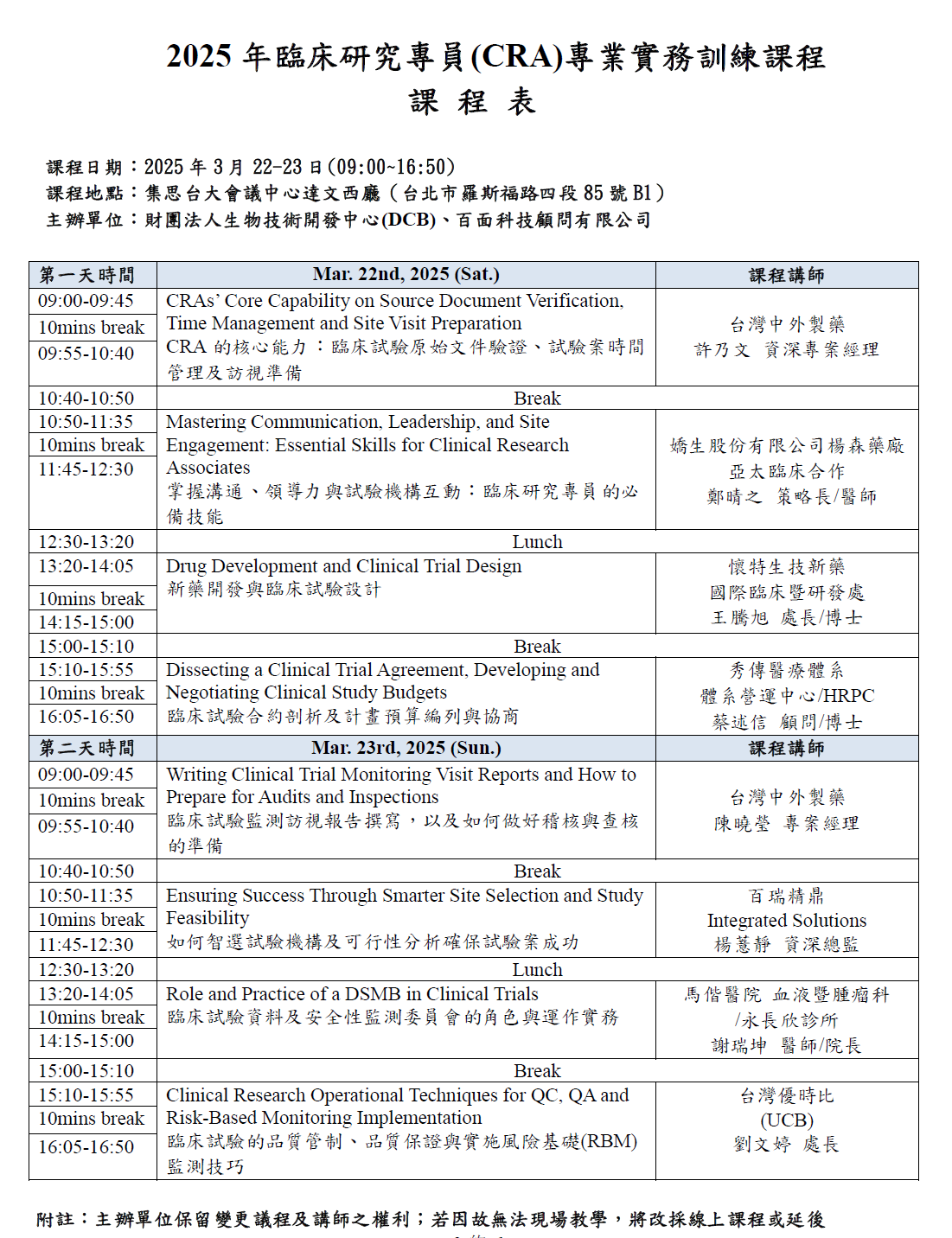
課程日期: 2025年3月22-23日(09:00~16:50)
課程地點:集思台大會議中心達文西廳(台北市羅斯福路四段85號B1)
主辦單位:財團法人生物技術開發中心(DCB)、百面科技顧問有限公司
報名時間:座位有限,額滿為止,最遲請於114/3/17 (一)前完成繳費,將以繳費順序保留座位權利
報 名 連 結:點我下載報名表
報名方式:e-mail、傳真或電話報名,Tel:02-2531-2198,Fax:02-2567-0069,
e-mail:
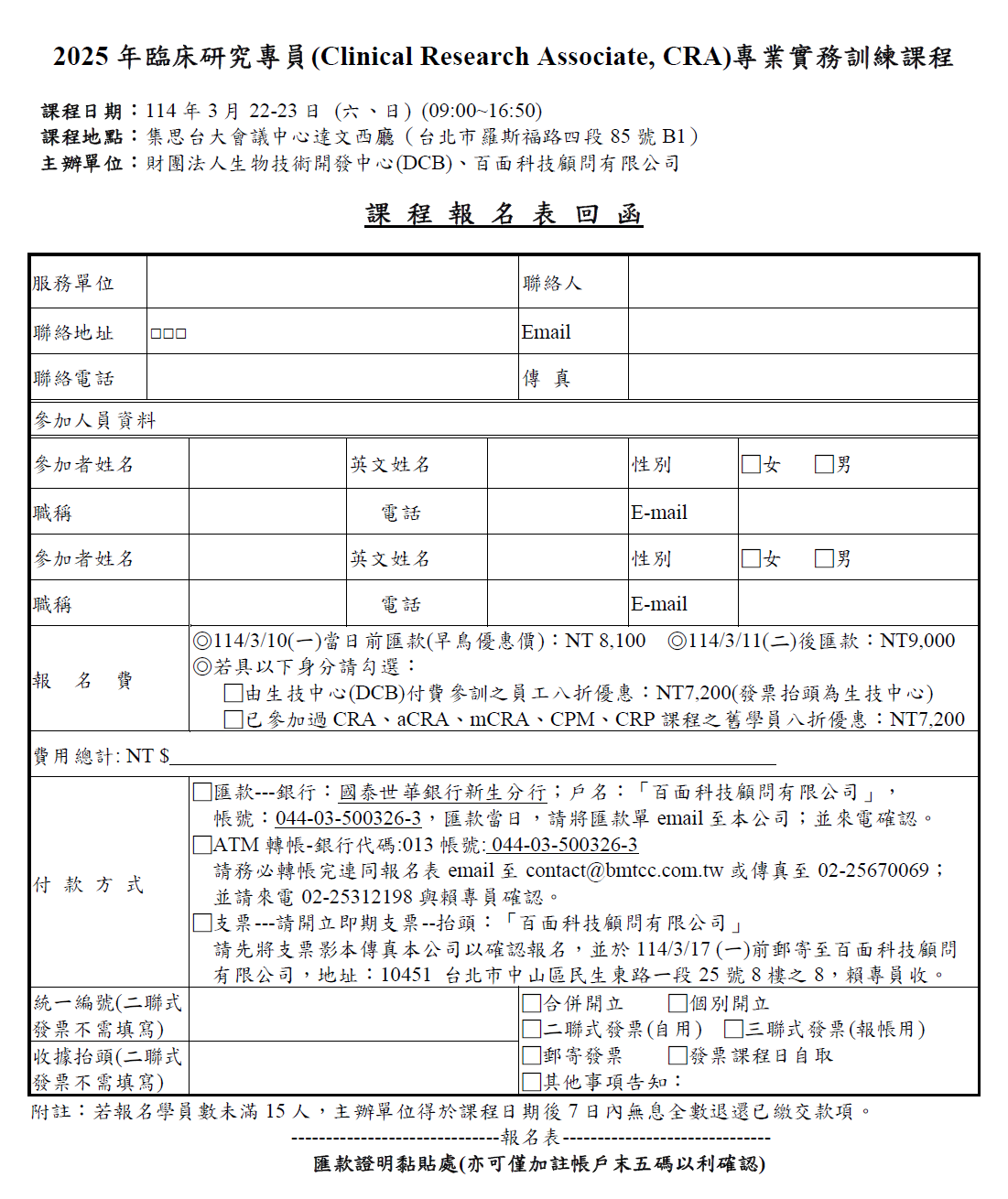
報 名 費: ◎114/3/10 (一)當日前匯款(早鳥優惠價): NT 8,100
◎114/3/11 (二)後匯款: NT9,000
◎生技中心(DCB)付費參訓之員工八折優惠: NT7,200
◎已參加過CRA、mCRA、CPM、CRP課程之舊學員八折優惠: NT 7,200
(以上均含講義、CRA工作手冊、精美中英文證書、早餐、中餐及茶點,小班教學名額
有限,已完成繳費者為優先順序,恕無提供停車優惠)
繳費方式:1.匯款或ATM轉帳--銀行:國泰世華銀行新生分行,銀行代碼:013
戶名:「百面科技顧問有限公司」,轉帳帳號:044-03-500326-3
2.支票:10451 台北市中山區民生東路一段25號8樓之8,賴專員收
注意事項:請於完成繳費後,將匯款單或轉帳收據連同報名表列印email或傳真至百面科技公司;
寄送支票者,也請先將支票影本及報名表列印後傳真至百面科技公司,並請來電確認
聯絡人員:賴專員 聯絡電話:02-2531-2198 傳真:02-2567-0069 電郵:
講師簡介:
許乃文:台灣中外製藥股份有限公司資深專案經理,曾任Pharmacia , sanofi-aventis藥廠、ICON、
PAREXEL 及 EPS等 CRO公司,具20年以上試驗案實施、監測管理之CRA經驗,國
立台灣大學藥理碩士
鄭晴之:嬌生股份有限公司楊森藥廠亞太臨床合作策略長/醫師,台大醫學士,美國哥倫比亞大學 MBA
,曾任台灣武田藥品工業醫藥事務部總監、台杉投資/水牛二號生物科技基金資深協理、嬌生
公司楊森藥廠亞太區臨床治療領域專家總監,GSK、NOVARTIS等國際知名藥廠高階醫藥學
術管理職務,具多件國際性臨床試驗案主導推動實務及優秀管理專長
王騰旭:現任懷特生技新藥國際臨床暨研發處處長,曾任職佳生科技顧問公司醫學科學部經理、嬌
生公司楊森藥廠醫藥學術部門、新加坡i3 research CRO、國防醫學院,以及台灣東洋、東
生華等藥廠臨床研究部門。Tim取得台大農化系生物工業化學組碩士及博士學位
蔡述信:任秀傳醫療體系體系營運中心/HRPC顧問、彰基第一至第三IRB專家顧問,具美國 ACRP
考試認證臨床試驗CCRC證照,任生技公司、多家醫學中心臨床試驗顧問,TFDA醫材諮詢
種子,曾任職佳生公司教育訓練中心經理、醫學中心臨床試驗中心、中研院生醫所專案經理、
經濟部商業司SIIR計畫主持人、衛福部 IRB查核委員,於香港大學臨床試驗中心主辦
Magnifier亞洲會議及國內多家大型醫院發表臨床試驗多場專業演講
陳曉瑩:台灣中外製藥股份有限公司專案經理,曾任專案副理及資深臨床研究專員,實際參與多件國
際性臨床試驗(Phase I - III,包含 First in Patient),以及Sponsor audit與TFDA inspection,
具有多年試驗案執行、監測管理之經驗,高醫大藥理學碩士
楊薏靜:百瑞精鼎Integrated Solutions資深總監,曾任職昆泰公司、嬌生公司、UCB、佳生科技等臨
床試驗相關產業,24年以上資深經驗,Cambridge University, Cambridge, UK, Pharmacology
Post-graduate research program,University of Sheffield, Sheffield, UK雙碩士,台大動物系學士
謝瑞坤:馬偕紀念醫院血液腫瘤科主治醫師、前主任、癌症中心主任,永長欣診所院長、國家衛生研
究院台灣腫瘤合作組織資料及安全監理委員會主席、台灣癌症全人關懷基金會董事長,國立
陽明大學醫學士,為國際知名臨床試驗計畫主持人(PI),具豐富臨床試驗計畫主持執行經驗
劉文婷:台灣優時比 (UCB)處長,曾任三顧生醫事業群副總經理、嬌生公司生物研究質量和合規部經
理,百靈佳殷格翰臨床試驗品質管理經理、CDE GCP查核小組長、資深專案經理、GSK
臨床試驗經理、美商惠氏藥品台灣區臨床試驗經理、MSD臨床試驗品質管控經理,高雄醫
學大學藥學士
 繁體中文
繁體中文  日本語
日本語  English
English 



